_Con estas vacunas se incrementa el número de candidatos (especialmente en mascotas) vacunas y especies a las que van dirigidas.
_Estas nuevas vacunas podrían estar en mercado en un plazo máximo de 3-4 años.
_Por un producto con ventas anuales de $25 Millones, BIONATURIS recibiría alrededor de $30 Millones durante los 10 primeros años de vida del producto.
_De aquí a 2016 se espera licenciar varios BNTs en cartera de cara a dar su salto al mercado.
1_ Evolución de los programas en desarrollo durante el 1º semestre.
2_ Estado y cuadro actualizado con nuevas vacunas en desarrollo desde el BNT014 al BNT022 (8 a mayores)
3_ Detalles y expectativas de recibir ingresos de los distintos BNTs
4_ ¿Cómo se puede valorar todo esto?
5_ Otros datos destacados.
6_ Repaso a otros datos ya conocidos de antemano.
1_Evolución de los programas en desarrollo durante este 1º semestre.
A nivel cualitativo los principales programas BNTs en marcha siguen según las previsiones en lo que respecta a los hitos técnicos y temporales. La importante apuesta por la expansión comercial internacional, reforzada recientemente con la incorporación de un Global Sales Manager afincado en EEUU, está dando sus frutos con el aumento del número de programas, de clientes y de potenciales clientes con los que la compañía se encuentra actualmente en negociación. Fruto de este trabajo se ha conseguido un primer contrato de relevancia en EEUU, con la compañía BMI, para el desarrollo del programa BNT014, un candidato a vacuna universal frente al virus del resfriado común en humanos, desarrollado por el sistema FLYLIFE. Se trata de un hito muy importante para la Sociedad a nivel estratégico ya que valida el sistema FLYLIFE en uno de los mercados más estrictos y competitivos del mundo.
En el marco de esta estrategia de expansión, tal como se publicó como hecho relevante en marzo de 2015, la Compañía se encuentra trabajando con el despacho de Carmelo Angulo Barturen para el diseño e implementación del plan de expansión en latino américa. Carmelo Angulo posee una amplia experiencia y conocimiento del mercado latinoamericano, habiendo ocupado puestos diplomáticos de alta relevancia en la zona. Entre otros cargos, ha sido embajador de España en México, Argentina, Bolivia y Colombia, además de coordinador residente de Naciones Unidas en Nicaragua y Argentina. Como parte del acuerdo, ya se ha realizado una primera misión comercial directa a México y próximamente se llevará a cabo otra a Colombia, Perú, Uruguay y Argentina. La Compañía se encuentra en negociación con las principales oportunidades generadas tras la primera misión comercial a México.
En lo que respecta a la expansión en Asia, la Sociedad comunicó el pasado 2 de julio la firma de un acuerdo estratégico con el Comité Administrativo de la Zona de Desarrollo Industrial de Alta Tecnología de la ciudad de Changshu (Jiangsu) – Changshu New & Hi-Tech Industrial Development Zone (CNZ)- para albergar una filial en el Parque Universitario de Ciencia y Tecnología de la región de Jiangsu (China), que servirá para desarrollar y distribuir activos biotecnológicos en el mercado asiático.
En la actualidad la Sociedad cuenta con una delegación comercial. Tras un intenso trabajo de prospección, desde el pasado mes de julio se están manteniendo reuniones con entidades de alta relevancia en el sector de salud animal en China, uno de los mercados de mayor crecimiento a nivel mundial.
Es de especial relevancia que la Sociedad está aumentando de manera importante los programas y oportunidades con entidades de tamaño menor que las grandes multinacionales pero que tienen alta capacidad de desarrollo, registro y fuerza de ventas en sus respectivos mercados de actuación.
En el ámbito de la división se informó igualmente al mercado el pasado 21 de julio del inicio del programa Bovihealth, junto a la entidad COVAP.
En el marco de este acuerdo se evaluará el efecto del programa BNT006 en ganado vacuno, dirigido a aumentar la productividad a través de la alimentación. BNT006 es un complejo peptídico inmunoestimulante y está alineado con la estrategia de la disminución del uso de antibióticos tradicionales en los ganados de explotación y consumo, declarado por las principales autoridades internacionales como unas de las principales actuaciones a seguir para frenar el fenómeno de resistencia a antibióticos. Fenómeno de alta trascendencia para la salud pública mundial.
2_Programas BNTs en desarrollo.
Para una mejor comprensión de este apartado, se incluye un caso general teórico ilustrativo del desarrollo de un compuesto biológico en el ámbito de salud animal:
_Hitos técnicos:
_Prueba de concepto (de fabricación y ensayos de eficacia y seguridad in vivo)
_Ensayos confirmatorios (ensayos clínicos de campo para medir seguridad y eficacia en la especie objetivo)
_Registro y comercialización
_Tiempo de desarrollo: 36-50 meses
_Costes de desarrollo: $ 3-6 Millones
BIONATURIS posible rol: desarrollador, fabricante y agente licenciante
_Ingresos por producto: por un producto con ventas anuales de $25 Millones, BIONATURIS recibiría alrededor de $30 Millones durante los 10 primeros años de vida del producto.
_Esquema de ingresos: cobros por desarrollo, licencia, cumplimiento de hitos y regalías por ventas.
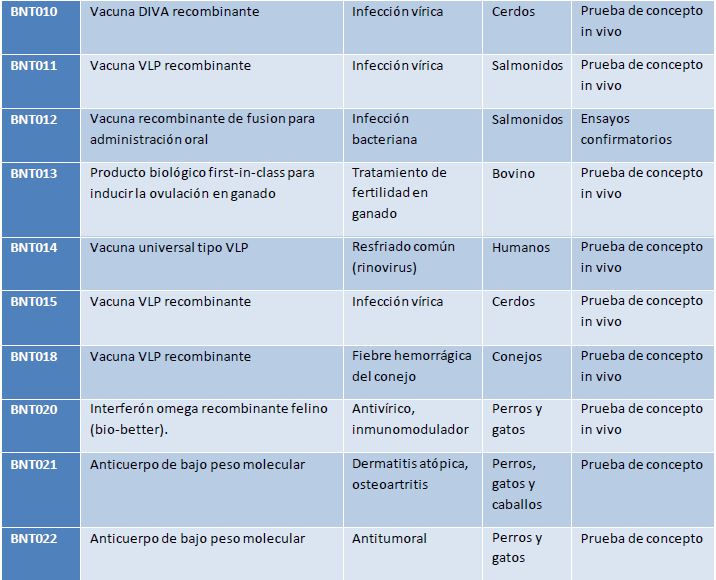
A continuación se muestra una tabla actualizada que recoge de manera resumida el estado de los programas autorizados para ser publicados.
3_ Detalles y expectativas de recibir ingresos de los distintos BNTs
De los productos incluidos en la tabla anterior 11 programas se encuentran en fase de prueba de concepto, 4 en fase de ensayos confirmatorios y 1 en fase de registro y comercialización.
BNT001 (biobetter para pacientes Gaucher Tipo I).
Versión oral de la enzima humana recombinante glucocerebrosidasa dirigida al tratamiento paliativo de pacientes Gaucher (humanos). BNT001 sería una versión oral alternativa a los tratamientos actualmente disponibles por infusión intravenosa.
Estado de desarrollo: Siguiendo las recomendaciones de la Agencia Española del Medicamento y Productos Sanitarios y la unidad de fase I del Hospital Universitario Virgen del Rocío de Sevilla se está ejecutando un plan de investigación preclínica.
Los experimentos de actividad in vitro de diferentes versiones de la enzima recombinante terminaron con la selección de una de las versiones como principio activo del candidato BNT001, con una actividad media de 400 unidades de glucocerebrosidasa por cada gramo procesado de las biofactorías vivas no fermentativas de Bionaturis. BNT001 rescata la actividad glucocerebrosidasa disminuida en fibroblastos de pacientes afectados por la enfermedad de Gaucher. El paquete preclínico avanzó con este candidato mostrando la capacidad de cruce de barrera intestinal en modelo in vitro e in vivo (rata) y resultando en valores de difusión y estabilidad aceptables para la continuación de las formulaciones orales. La farmacocinética completada en modelo murino también avala la formulación oral. Sin embargo, no se ha identificado hasta la fecha cruce de la barrera hematoencefálica, por lo que continua la investigación para conocer si aparte de la enfermedad de Gaucher tipo I, el candidato se podría proponer para las versiones neuronopáticas de la enfermedad, tipos II y III. Esto hace que sigan los experimentos en modelo murino y se posponga la entrada en modelo no roedor hasta Q3-2016.
Llegada esperada al mercado: indeterminada
Fecha esperada para obtener ingresos: 2016-2017 derivado de acuerdo de licencia con sponsor.
BNT004 (vacuna recombinante para combatir nematodos intestinales en ganado).
Eficacia, efectividad y seguridad evaluada en modelo de ratón contra una especie de parásito y en corderos en condiciones de infección con distintas especies de alta incidencia. Se trataría de la primera vacuna profiláctica para la prevención de este tipo de infecciones parasitarias.
Estado de desarrollo: una compañía multinacional se encuentra validando la eficacia y seguridad de la vacuna en un ensayo experimental en corderos bajo condiciones específicas de infección de interés estratégico para la compañía. Los resultados del ensayo de prueba de concepto bajo estas condiciones realizados durante 2014 muestran que la vacuna es segura, crea una respuesta inmune contra al menos 3 especies distintas, reduce la cantidad de parásitos y los huevos depositados por éstos. Para buscar mejorar la respuesta a nivel de mucosa y disminuir la incidencia de parásitos y huevos en condiciones de campo se debe continuar con un ensayo dosis-respuesta que incluya distintas variaciones de las condiciones de formulación final, incluyendo adyuvantes. La fecha de inicio del nuevo ensayo sigue pendiente de aprobación por parte del sponsor.
Fecha esperada de llegada al mercado final: dependiente de la fecha de inicio de nuevo ensayo.
Fecha esperada de generar ingresos: dependiente de la fecha de inicio de nuevo ensayo.
BNT005 (vacuna recombinante, profiláctica y terapéutica, frente a leishmaniasis visceral canina).
BNT005 sería la primera vacuna recombinante que no depende del parásito para su fabricación y que induce el mismo tipo de respuesta inmune observada en los individuos que superan la enfermedad, sirviendo no solo para prevenir, sino para tratar esta enfermedad canina.
Estado de desarrollo: eficacia y seguridad demostrada en retos en modelo de ratón transgénico humanizado. Tras el periodo de selección del candidato en modelo murino, BNT005 ha superado los objetivos de una primera prueba de concepto en perros Beagle (2013) que incluyó ajuste de dosis (seguridad y eficacia en la generación de respuesta inmune) y un segundo ensayo aumentando la cantidad de perros Beagle, incluyendo la selección de adyuvante (2014). Los resultados confirmaron seguridad y eficacia en la generación de la respuesta inmune humoral y celular deseada en todos los perros inmunizados, así como la eliminación de parásitos en algunos individuos que se infectaron de forma natural previa al ensayo. En Q2-2015 comenzó el primer ensayo de infección experimental de los perros naive inmunizados en 2014, para evaluación de mantenimiento de la respuesta tras la infección y protección frente al desarrollo de la enfermedad. Los resultados obtenidos hasta la fecha muestran éxito en alcanzar el primer objetivo ya que el parásito no ha sido capaz de revertir la respuesta inmune inducida por la vacunación e induce la respuesta asociada a enfermedad en los perros no vacunados. El ensayo continua hasta al menos final de 2015 para observar si se alcanza el segundo objetivo (protección) y los perros vacunados no desarrollan los síntomas de la enfermedad. Validado y monitoreado por una compañía multinacional, se planifica conjuntamente un ensayo final de eficacia frente a infección natural con alto número de individuos en zona endémica para la enfermedad a comenzar en Q2-2016.
Fecha esperada de llegada al mercado final: La vacuna podría llegar al mercado al final de 2017.
Fecha esperada de generar ingresos: Durante la primera mitad de 2016 como resultado de ejecución de derecho de licencia.
BNT006 (péptido antimicrobiano).
Péptido antimicrobiano para combatir infecciones y sus efectos sin el uso de antibióticos o esteroides, incluyendo bacterias multirresistentes. Uso aislado o de manera combinada con otros agentes bactericidas. Mecanismo de acción bactericida diferente al de los antibióticos tradicionales. Aplicación en salud humana, animal y como agente bactericida en la industria.
Estado de desarrollo: Tras los resultados en ensayos in vitro mostrando el mismo efecto bactericida que una referencia comercial, se están completando ensayos de eficacia y toxicidad en distintos modelos animales mediante tratamiento oral. Los resultados indican una actividad general inmunoestimulante en ensayos in vivo, responsable del incremento de parámetros de crecimiento y disminución de señales de estrés en los animales. Los resultados de estos ensayos se completarán en Q4-2015 y durante el trimestre comenzará un ensayo de uso en bovino en condiciones de granja de producción.
Fecha esperada de llegada al mercado final: 2016.
Fecha esperada de generar ingresos: 2016 como resultado de ejecución de derecho de licencia.
BNT007 (vacuna recombinante para aves).
Vacuna recombinante multivalente para aves, contra cepas clásicas y variantes muy virulentas de un virus de alta incidencia como son la enfermedad de gumboro y newcastle
Estado de desarrollo: Tras la puesta a punto de la producción del producto final en Bionaturis, destinado a paliar los efectos de la incidencia de nuevas variantes del virus en granjas de producción en México, los ensayos de eficacia y toxicidad en aves domésticas estaban programados para Q3-2014 en granjas experimentales de México. Los ensayos en granjas se retrasaron por problemas de importación ya resueltos, pero se han vuelto a retrasar por la crisis de gripe aviar en Norteamérica agudizada desde Q2-2015. Se espera comienzo de ejecución en Q1-2016.
Fecha esperada de llegada al mercado final: 2017.
Fecha esperada de generar ingresos: 2016-2017 como resultado de ejecución de derecho de licencia.
BNT010 (vacuna recombinante para cerdos). Vacuna recombinante DIVA para ser aplicada en cerdos.
Estado de desarrollo: BNT010 es un producto alternativo a vacunas comerciales utilizadas para prevenir y controlar una importante enfermedad porcina con incidencia global. BNT010 introduce la posibilidad de fabricación del número justo de dosis para controlar brotes de la enfermedad en cualquier región, solventando los problemas de fabricación y suministro de las alternativas comerciales. Tras el desarrollo del proceso de fabricación, los resultados de ensayos in vivo obtenidos en Q4-2014 en colaboración con una multinacional mostraron similares y/o mejores resultados que las referencias comerciales. El producto está en negociación con organismos gubernamentales de distintos continentes cuya misión es proteger la cabaña porcina en regiones estratégicas de incidencia de la enfermedad. Además, en el último trimestre Bionaturis ha adaptado el principio activo de la vacuna para obtener una formulación apta para su uso en el diagnóstico de la enfermedad.
Fecha esperada de llegada al mercado final: 2016-17.
Fecha esperada de generar ingresos: 2016 como resultado de ejecución de derecho de licencia.
BNT011 y BNT012 (vacunas para salmón 1 y 2).Vacunas recombinantes para administración oral para salmones de acuicultura.
Estado de desarrollo: BNT011 es una vacuna contra una enfermedad viral y está en proceso de selección del candidato final en colaboración con un prestigioso laboratorio europeo especializado en virus de interés en acuicultura. BNT012 es una vacuna contra una importante enfermedad bacteriana y es objeto de un acuerdo de evaluación y opciones con una importante multinacional veterinaria, que está realizando los ensayos de evaluación en salmones tras el desarrollo de la fabricación en Bionaturis.
Los resultados finalizados en 2014 mostraron seguridad y eficacia en la reducción significativa de la enfermedad en salmones infectados experimentalmente. Sin embargo, se detectó la necesidad de ajustar la dosis para aumentar el efecto de la vacunación en la supervivencia de los salmones retados. En la primera mitad de 2015 Bionaturis ha optimizado la fabricación de lotes y comenzó el segundo ensayo en salmones en Q2-2015 tras la liberación de recursos en las instalaciones homologadas (Chile). Tras la aclimatación de los salmones al ensayo, la vacunación comenzó en Q3-2015 y el ensayo finalizará en Q4-2015.
Fecha esperada de llegada al mercado final: 2016.
Fecha esperada de generar ingresos: 2016 como resultado de ejecución de derecho de licencia.
BNT013 (tratamiento fertilidad del ganado).
Medicamento novedoso fabricado mediante FLYLIFE, dirigido a inducir la ovulación del ganado previo a la inseminación artificial. Objeto de un contrato de desarrollo con una multinacional veterinaria, Bionaturis ejecutará las pruebas de eficacia y seguridad del nuevo fármaco en modelos animales, mientras que la multinacional validará estos resultados en sus instalaciones en ensayos de campo con la especie objetivo. El acuerdo incluye opciones de derecho de licencia en exclusiva a favor de la compañía multinacional.
Estado de desarrollo: Prueba de fabricación exitosa en sistema FLYLIFE. Los resultados previstos para Q2-2015 fueron completados. Se realizaron sobre tejido derivado de gónadas animales y fueron ejecutados por uno de los principales expertos en reproducción en España. Mostraron que esta nueva molécula de diseño, primera en su género y desarrollada completamente en Bionaturis, posee actividad inductora de la producción de testosterona, progesterona y estradiol, similar o superior que las hormonas naturales. Los ensayos de conformación se han completado con éxito en colaboración con un experto en hormonas de la reproducción en Francia. Los resultados de inducción de ovulación en modelos animales se están ejecutando y se completarán en Q3-2015. Tras ello, el producto pasará a ser ensayado en la especie objetivo durante el próximo ciclo reproductivo del ganado bovino en Brasil en Q1-2016, año en el que Bionaturis fabricará el lote piloto homologado para los ensayos destinados al registro del producto.
Fecha esperada de llegada al mercado final: 2018.
Fecha esperada de generar ingresos: desde la firma del contrato la compañía multinacional está abonando a Bionaturis los costes de desarrollo. Se esperan otros ingresos a partir de 2016 como resultado de ejecución de derecho de licencia en caso de resultado positivo en ensayos de campo en especie objetivo.
BNT014 (vacuna universal contra virus del resfriado común en humanos).
Vacuna recombinante de diseño destinada a proteger contra la mayoría de serotipos de rinovirus humano, causante del resfriado común y sus efectos globales de incidencia en salud y en la economía. La vacuna ha sido diseñada por la empresa Biological Mimetics (Maryland, EE.UU.) utilizando su tecnología IRT (Immune Refocusing Technology). Esta tecnología introduce cambios en la secuencia de las proteínas de la superficie del virus para que el individuo vacunado cree inmunidad contra la mayoría de las variantes de este virus, uno de los que cambia con más facilidad para escapar del sistema inmune y contra el que no se ha podido desarrollar una vacuna hasta la fecha. Parte del desarrollo de este producto está financiada por los institutos de salud de los EE.UU. (NIH) con el objetivo de completar la preclínica en 2017 y ensayos clínicos Fase I con voluntarios sanos en 2018.
Estado de desarrollo: La fabricación de la vacuna basada en una de las proteínas de superficie del virus y ensamblada con la forma de la cápsida del virus original es un reto tecnológico que ha sido solventado por Bionaturis. Desde Q2-2015, Bionaturis envía lotes experimentales de dos alternativas de la vacuna a Biological Mimetics para ensayos de estabilidad y eficacia en neutralización de variantes de rinovirus humano. Los resultados preliminares de fabricación han permitido diseñar un protocolo de escalado industrial de BNT014, mientras que los resultados preliminares en modelos animales muestran la neutralización de variantes de rinovirus distribuidas por todo el árbol filogenético del rinovirus humano mientras que vacunas basadas en virus inactivados solo neutralizan el serotipo del virus usado en la vacuna.
Fecha esperada de llegada al mercado final: 2021.
Fecha esperada de generar ingresos: desde Q3-2015 Bionaturis recibe fondos de un programa para el desarrollo de esta vacuna financiado por el gobierno de EE.UU. Se esperan otros ingresos a partir de Q3-2016 como resultado del desarrollo al completar hitos en el proceso de desarrollo clínico de la vacuna.
En el informe detallan hasta el BNT14, sin embargo gracias a nuestras investigaciones podemos aportar datos del BNT018 y BNT020, la empresa debería enviar un HR adicional completando el cuadro desde el BNT015 al BNT022.
BNT018: vacuna recombinante contra Enfermedad Hemorrágica del Conejo (RHD)
BNT018 es una vacuna recombinante contra virus RHD basado en partículas similares a virus (VLPs) formadas por la proteína VP60 viral. BNT018 podría sustituir las vacunas muertas clásicos. Las VLPs fueron producidos con altos rendimientos en una plataforma no fermentativa entrega de 90 dosis por gramo de peso fresco de biofábricas procesados viviente. Una dosis efectiva seroconvirtieron conejos 7 días después de la inmunización y dio lugar a 100% de protección después de la infección de los conejos.
La eficacia y la toxicidad probados y confirmados en conejos infectados. La vacunación incremento en todos los conejos el numero de anticuerpos. Los animales vacunados no mostraron ningún síntoma de la enfermedad después del desafío.
Se encuentra en pruebas preclínicas.
BNT020: Interferón Omega recombinante de Origen felino
BNT020 es una versión mejorada del Interferón omega de origen felino aprobado para el tratamiento de las infecciones por parvovirus en los perros y los virus de la leucemia felina y el virus de la inmunodeficiencia felina en gatos. BNT020 incorpora cambios en la secuencia Interferón Omega y también en el proceso de fabricación aunque todavía usando biofábricas vivos, para entregar un producto con 5 veces la actividad del producto ya comercializado, basado en un ensayo in vitro de inhibición de virus de la estomatitis vesicular (VSV) en células de riñón de gato (CRFK).
BNT020 está listo para llevar a cabo pruebas de campo fundamental para el registro
Como “curiosidad” cada caja de Interferon Omega de Virbagen tiene un precio de mercado de 414,65€
http://www.farmaciaveterinaria.es/index.php?main_page=product_info&cPath=12_34_56&products_id=927
4_ ¿Cómo se puede valorar todo esto?
IMB GROUP recientemente publico un articulo indicando como valorar una empresa BIOTECNOLOGICA pura ,el resumen podría ser el siguiente.
Una empresa de biotecnología como una colección de uno o más fármacos experimentales, cada uno representando una oportunidad de mercado potencial. La idea es tratar a cada fármaco prometedor como una mini-empresa dentro de una cartera. Mediante un análisis de DCF (flujo de caja descontado), se puede determinar lo que alguien estaría dispuesto a pagar por esa cartera de medicamentos.
Previsiones de ingresos: La previsión de los ingresos por ventas de cada una de los proyectos de una compañía de biotecnología es probablemente la estimación más importante que se hace acerca de los flujos de efectivo futuros, pero también puede ser la más difícil. La clave es determinar qué total de ventas se lograría si por ejemplo, un fármaco hace todo el camino a través de los ensayos clínicos de forma exitosa. Normalmente, se pronostican las ventas durante los primeros 10 años de vida del fármaco.
Mercado potencial: Se empieza por hacer suposiciones sobre el potencial de mercado del fármaco mediante la información proporcionada por la empresa y los informes de investigación de mercado para determinar el tamaño del grupo de pacientes que lo usarán (prevalencia e incidencia). Los analistas suelen centrarse en el potencial de mercado en los 7 grandes mercados farmacéuticos (USA, Japón, UK, Francia, Alemania y España), seguidos cada vez más de cerca por los mercados emergentes (BRiC’s y otros).
Probabilidades de éxito: El riesgo disminuye a medida que el medicamento va pasando de fases.
Según un estudio americano de Investigadores y Fabricantes Farmacéuticos los medicamentos en Fase I de ensayos clínicos tienen una probabilidad del 15% de convertirse en un producto comercializable.
Para los de la Fase II, las probabilidades de éxito aumentan al 30%,
y para la Fase III, suben al 60%.
Una vez que los ensayos clínicos son completados y el fármaco entra en la fase final de aprobación de la FDA (Food & Drug Administration, la agencia del gobierno de los Estados Unidos responsable de la regulación de alimentos, suplementos alimenticios, medicamentos, cosméticos, aparatos médicos, productos biológicos y derivados sanguíneos), tienen un 90% de probabilidades de éxito. Estas mejoras en las probabilidades de éxito se traducen directamente en un aumento del valor de las acciones.
Al multiplicar el free cash flow estimado de cada fármaco por la probabilidad de éxito correspondiente a la fase en que se encuentre, se obtiene una previsión de free cash flows que tienen en cuenta el riesgo de desarrollo. El siguiente paso es descontar los flujos futuros que se esperan en los próximos 10 años para determinar el valor actual. Debido a que ya toman en cuenta en el riesgo de éxito anteriormente, no es necesario incluirlo en la tasa de descuento. Se utiliza el enfoque del coste promedio ponderado del capital (WACC). Éste método se conoce como rNPV (risk-adjusted Net Present Value), Valor Presente Neto ajustado por Riesgo.
¿Cuál es el Valor de la empresa?
Por último, se quiere calcular el valor total de la empresa de biotecnología. Una vez calculado el flujo de caja descontado para cada uno de los medicamentos de la empresa biotecnológica, se suman para obtener un valor total de la cartera de medicamentos de la empresa.
DCF Valor Producto A + DCF Valor Producto B + DCF Valor Producto C … = Valor total de la empresa
Conclusiones
Se podría decir que el proyecto es inicialmente casi invalorable, ya que es difícil poder poner un precio a algo que se debe desarrollar y que normalmente no seguirá el plan establecido, y que estadísticamente hablando, las posibilidades de éxito son muy pocas. De hecho, el valor del proyecto al comenzar podría ser cero.
http://imbgrup.com/web/como-valorar-a-una-empresa-de-biotecnologia-pura/
BIONATURIS hace vacunas principalmente para animales (19/22), por ello se puede decir lo siguiente:
Los que llevan un desarrollo menos avanzado como el BNT08 (Lubinas) o el 16-17 y 19 ya no se tienen en cuenta, solamente los que tendrían la posibilidad manifiesta de llegar a mercado.
Por ello a sus 2 vacunas de humanos se le podría dar una posibilidad de un 15% (Rinovirus y Gaucher), 9 vacunas con probabilidad de éxito de llegar a mercado del 30%, 4 vacunas con probabilidad de éxito del 60% y tendría 1 con probabilidad de éxito del 90%,
Si solo nos centramos en los mas “avanzados podríamos deducir lo siguiente.
Partiendo de la base uno de los mas prometedores es el BNT05 (espera licenciarse en el 1º semestre de 2016) , el medicamento de VIRBAC o el Jarabe que hay actualmente para la Leishmaniasis no son efectivos.
Esto es lo que actualmente se comenta de la vacuna de VIRBAC canelish, que no funciona y competiría con BIONATURIS.
La vacuna protege frente a la enfermedad clínica, NO FRENTE AL CONTAGIO.
Por tanto UN PERRO VACUNADO PUEDEN ENFERMAR DE LEISHMANIA.
El Protocolo de aplicación es el siguiente: previo análisis para descartar que el perro esté infectado ya por leishmania el calendario de vacunación consiste en una primovacunación ( a partir de los 6 meses de edad ) en la que se pondrán 3 dosis de vacuna separadas a inteRvalos de 3 semanas cada dosis.
La inmunidad final aparece 4 semanas después de la última dosis. Después será necesaria una revacunación anual una sola dosis para mantener la inmunidad.
Precio aproximado:
El precio del test es de 25 €.
El precio de cada dosis de vacuna es de 54 € por dosis.
Test y las tres dosis de la primera vacunación por: 187,00€
Las únicas forma de PREVENIR EL CONTAGIO son PIPETAS Y COLLARES que impiden que el flebótomo pique a tu perro, por tanto ni la vacuna ni el jarabe PREVIENEN EL CONTAGIO.
Este hecho se puede ver en el siguiente articulo: http://uprocanes.es/la-polemica-sobre-la-vacuna-de-la-leishmaniosis/
En el 1º año de comercialización en EUROPA Canelish vendió un total de 1 millón de dosis de la vacuna y se vacunaron 300,000 perros (se necesitan 3 dosis por perro) http://argos.portalveterinaria.com/pdf/bionews_10.pdf
Por ello dando un precio medio de unos 40€ se podría cifrar en EUROPA en unos 40 millones de € , a esto habría que añadir EEUU y Asia, por ello podríamos determinar unas ventas globales de mas de 150 millones de €.
Pues bien, el BNT05 competiría con canelish y el jarabe, de ser efectiva como indican podría tener una penetración importante porque tanto el Jarabe como la vacuna de Virbac no valen y los medicamentos como veréis no son baratos…
Teniendo en cuenta una tasa de penetración del producto de un 30-40% de cuota de mercado, se estimaría en 45-60 millones las ventas a nivel global, de los cuales un 12,5% neto anual iría a parar a la caja de BIONATURIS.
Esto supondría fácil para BIONATURIS entre 5 y 7,5 millones de € netos al año para la compañía. Durante los 10 primeros años.
A esto habría que añadir lo de los salmones (BNT011) vacuna oral para el ISA, que una vez llegue a mercado la empresa estimaba entre 1 y 1,5 millones de € netos al año para la compañía. Durante los 10 primeros años 10/15M de €.
Con estos 2 es suficiente para dar un valor a la empresa según la fórmula “standart” de valorar empresas comentada anteriormente de unos 80 millones de € , lo que supondría incluida la AK pendiente valorar la compañía en unos 15€ por acción. A partir de aquí habría que hacer lo mismo con los otros 20.
Es algo que se podría hacer pero valiendo 5€ no vale la pena puesto que es obvio que vale más.
Ventas estimadas en caso de llegar mercado / probabilidad de que dicho medicamento llegue a mercado…
Y es algo que no vale la pena porque el posible precio objetivo se dispararía muy por encima de los 100€…
Valorar la compañía de otro modo supondría una valoración errónea
Toda valoración sin tener en cuenta los desarrollos, estado de los mismos y ventas futuras es errónea puesto que no es la forma “standart” correcta para valorar a una empresa de este tipo.
El método de valoración justo y real es el standart, si no que se lo digan a Alexion., por Synageva este año se pagaron en una OPA 8400 millones de $, una prima de un 140% por una empresa en perdidas y que no vendía nada, simplemente tenia productos en desarrollo y para enfermedades raras. ( ver link )
5_ Otros datos destacados:
NIH (National Institute of Health). Son muy pocas las empresas de fuera de USA que contratan con ellos y españolas mucho menos. No es fácil entrar en ese grupo selecto. http://www.nih.gov/ y BIONATURIS esta en él.
La filial está actualmente en constitución en los EEUU como fue informado mediante HR ,en EEUU.
En este sentido en Junio de 2015 BIONATURIS ha fichado a Eli kehrli
Gerente de Ventas Global del grupo Bionaturis desde junio de 2015 – Actualidad (4 meses)
• Administra el equipo de ventas para alcanzar las metas de ganancias y ventas globales.
• Diseña programas de ventas y marketing y establece estrategias de ventas a corto y largo plazo.
• Dirige el trabajo del equipo de ventas de las diferentes filiales que componen BNT.
• La promoción, la comercialización y la venta directa de productos / servicios en todo el mundo.
• Negociación de contratos con clientes y propuestas de servicios.
A su vez ha estado al frente de empresas con mas de 10000 empleados incrementando a doble dígito las cifras año a año mientras ha estado al frente.
https://www.linkedin.com/in/elikehrli
China: Su implantación se ha producido en el 3º trimestre (julio de 2015) y los BNTs se están incrementando de manera exponencial con socios locales chinos como el BNT018 y el BNT020
En ambos casos los hitos alcanzados no se reflejaran como es obvio hasta el 2º semestre de 2015.
Los Animales, son el nuevo negocio de las farmacéuticas.
Grandes fabricantes de medicamentos, entre ellos Zoetis, Novartis y Bayern ven en medicinas para animales un gran mercado en crecimiento:
Pasen y vean…
Una empresa como BIONATURIS que capitaliza 20 millones de € es una golosina para cualquier multinacional… estas últimas pierden patentes y los miles de millones que ganan lo utilizan para comprar empresas mas pequeñas que le sirvan para incorporar productos a su cartera.
Por muy poco se puede comprar la empresa entera.
Algo que suele pasar cuando las biotecnológicas tienen productos listos para salir al mercado.
BIONATURIS cuenta con una buena mano.
Esta empresa no es una compañía que se esté jugando todo a 1 sola carta, si así fuera se trataría de un casino a cara o cruz puesto que con 1 sólo desarrollo, si este se cae, adiós empresa. Aquí se está jugando con un portfolio de 22 vacunas en desarrollo, de las cuales 1 está en registro previo, 4 con ensayos confirmados (previo al registro) , 11 en prueba de concepto y unas 6 en un estado de desarrollo menor….
Estadísticamente hablando los 8 BNTs nuevos anunciados en este HR garantizan al menos 1 nuevo producto en mercado.
https://www.bolsasymercados.es/mab/esp/EE/HechosRelevantes.aspx
6_ Repaso a datos conocidos de antemano.
Cualquiera que haya leído nuestro informe cuando descubrimos datos de varios BNTs nuevos con el socio local Chino estará al día de la actualidad de la empresa.
1_ Los ingresos correspondientes al acuerdo de BMI y la entrada en China corresponden al 3º y 4º trimestre y no al 1º y 2º, ambos acuerdos fueron cerrados a final de semestre/ principio del 2º semestre, por tanto en las cifras de la empresa no entran estos nuevos hitos.
2_ Tener 8 vacunas nuevas en desarrollo implica como dice la empresa en el cuadro un mayor gasto, cada vacuna en desarrollo para animales tiene un coste entre 3-6 millones de € y tarda entre 3-4 años en llegar al mercado (plazo mucho mas breve que en vacunas para humanos) si no que se lo digan a ZELTIA que aun sigue detrás de la aprobación de la FDA del Yondelis.
3_ La empresa espera unos ingresos de explotación de 2,37 millones de € a cierre de ejercicio (sin contar la compra) vs los 2,55 millones que calculamos, por ello estas previsiones están totalmente en línea y descontadas. En el HR indican que esta cifra podría ser superior por que hay cosas que pueden salir a final de año como retrasarse a comienzos de 2016, por prudencia no las han incluido.
4_ La compra sigue aplazada hasta el 30 de noviembre, desde la empresa nos comentan que han querido ser prudentes por eso no han concretado cifras futuras aun este 11 de septiembre, indican que podría haber noticias en próximos días como alargarse más, de ahí que para evitar malos entendidos dejarán la fecha prevista en el fin de la prorroga de la AK 30 de noviembre.
5_La compra como dijo el presidente en expansión no peligra, además una vez cerrada la misma los ingresos de explotación serán los estimados superando 9M en 2016 con 3M de EBITDA , de hecho las previsiones a futuro no cambian.
6_Esta compra no ofrece un potencial de crecimiento significativo a la empresa , porque nada tiene que ver con la propia actividad de BIONATURIS que es la que dará el dinero, sirve para asegurar unos ingresos recurrentes que actualmente no tiene.
Los ingresos de la empresa hasta que reciba (royalties) y posteriormente un porcentaje de las ventas, no son fijos, hoy puede aparecer una farmacéutica y pagar X por desarrollar una vacuna, pero no es recurrente puesto que se paga 1 vez y no tienen por que repetirse a corto plazo. De ahí que los ingresos provenientes de la entrada en China como lo del Rinovirus entrará en este 2º semestre, que es donde se pegará el salto.
7_ Luego volvemos a lo de siempre y que no tiene arreglo: mientras otras empresas sacan una patente y mandan un HR especifico con dicha patente y suben un 40% en bolsa, en BIONATURIS publican 8 nuevos desarrollos y lo publican en un documento de resultados que nadie pasará de la 1º hoja y de este modo pierden visibilidad, no obstante esto no cambia la realidad de la empresa.
Si los que llevan la comunicación de NEURON BIO lo hicieran en BIONATURIS ahora mismo valdría la acción mas de 15€, pero sin ninguna duda….
Esto también es una señal que el equipo directivo no esta obsesionado con la subida de la acción, saben que en cuanto vayan saliendo cosas empezará a subir.


[…] Y este es el traducido al español: https://www.gesprobolsa.com/bionaturis-hr-desarrollara-8-nuevas-vacunas/ […]
[…] Y este es el traducido al español: https://www.gesprobolsa.com/bionaturis-hr-desarrollara-8-nuevas-vacunas/ […]