_Entender una empresa biotecnológica.
_El BNT05 nuevos datos, casi a punto.
_Resto de Portfolio y detalle de “los Top”
_Resultados 2015 en línea con las previsiones.
_Entender una empresa biotecnológica.
Una empresa Biotecnológica no es una empresa “al uso”, por ello recomendamos leer este articulo siempre antes de invertir en cualquier empresa del sector. https://www.gesprobolsa.com/bionaturis-neuron-bio-oryzon-zeltia-el-ciclo-de-vida-de-una-biotecnologica/
Aquí hay otro artículo: http://imbgrup.com/web/como-valorar-a-una-empresa-de-biotecnologia-pura/
Si no se comprende lo anteriormente descrito, lo mejor es buscarse otro sector.
Un resumen lo mas breve posible:
Ensayos clínicos (Fase I) 15% de éxito
Ensayos clínicos avanzados (Fase II) 30% de éxito.
Ensayos clínicos finales (Fase III) 60% de éxito.
Entrada en registro y fase de aprobación por parte de las autoridades reguladoras- 90% de éxito. Y aquí es donde BIONATURIS tiene casi 2 de los 23 actualmente en portfolio, entre ellos el BNT05 según datos publicados.
Por ser todavía mas claros, recientemente Pharmamar (ExZeltia) dio resultados, en los mismos se ve un gasto de I+D importante por avances en sus desarrollos. El viernes el mercado entendió dicho aumento de gasto en I+D como una seria posibilidad de tener que realizar una ampliación de capital a futuro para costearse los ensayos.
Todo ello pese a que la empresa pretende comercializar Aplidin este año, si eso se consigue, no sería necesario ampliar capital de nada por que los ingresos que entrarían de golpe en caja serán suficientes como para cubrir todo el gasto en I+D.
Rovi es otro caso peculiar, sin ser BIOTECNOLOGICA si que esta invirtiendo mucho en I+D de cara a la aprobación de la enoxaparina , si consigue sacar ese producto al mercado, la empresa estima que sus ingresos, EBITDA y resultado neto se doblaran.
Es decir que pasaría de unos 250 millones de ingresos anuales a 500 millones de €, pasaría de un EBITDA de unos 32 millones a cerca de 70 millones de € y un beneficio neto superior a los 40 millones de €, dicho por su presidente y ROVI no es dudosa.
http://cincodias.com/cincodias/2015/04/16/empresas/1429177834_493580.html
Mas que ver que gana o pierde la empresa en el momento actual , en este sector hay que ver cuanto se puede generar que una vacuna llegue al mercado, esa es la verdadera clave, como dijo el presidente de ROVI el hecho de tener una vacuna mas en mercado le supondrá 250m en ingresos ,unos 35m de EBITDA y unos 20m de € de neto.
Aquí en BIONATURIS no se da valor a los 23 desarrollos que hay en cartera, simplemente por que no se entiende el concepto planteado al principio, lo destacado en BIONATURIS es la posibilidad de licencia de 6 vacunas este mismo año y 2 en registro que eso ya es probabilidad del 90% , ahí los ingresos ya no serán los que son, una aprobación por parte de un regulador + acuerdo de licencia + comercialización suponen garantizarse millones y millones de € de ingresos recurrentes cada año.
Además como mostraremos a continuación en Resultados 2015 auditados, a diferencia de lo ocurrido en Pharmamar, BIONATURIS indica que tiene capacidad financiera y puede hacer frente a las necesidades de inversión en Gastos de I+D para mantener y ampliar su capacidad tecnológica.
No tiene necesidad de ampliar capital a corto plazo.
Recordemos que el jueves se informo al mercado la formalización de la operación con el fondo INVEREADY que entrará en la compañia con un 5% del capital social. https://www.gesprobolsa.com/bionaturis-hr-inveready-se-hace-con-del-5-del-capital/
_El BNT05 nuevos datos, casi a punto.
_La clave por la capacidad importante de generar ingresos esta en el BNT05, el comunicado de la presentación de resultados es claro, la vacuna es efectiva y mejora todo lo que hay en mercado, la licencia y posterior comercialización parecen estar cerca.
BNT005 (vacuna recombinante, profiláctica y terapéutica, frente a leishmaniasis visceral canina).
BNT005 sería la primera vacuna recombinante que induce el mismo tipo de respuesta inmune observada en los individuos que superan la enfermedad, sirviendo no solo para prevenir, sino para tratar esta enfermedad canina.
Tras el periodo de selección del candidato en modelo murino, BNT005 superó los objetivos de una primera prueba de concepto en perros Beagle (2013) que incluyó ajuste de dosis (seguridad y eficacia en la generación de respuesta inmune) y un segundo ensayo aumentando la cantidad de perros Beagle, incluyendo la selección de adyuvante e investigación de su contribución a las propiedades de la vacuna, la cual se diseñó para no necesitar de adyuvante (2014). Los resultados confirmaron seguridad y eficacia en la generación de la respuesta inmune humoral y celular deseada en todos los perros inmunizados, así como la eliminación de parásitos en algunos individuos que se infectaron de forma natural previa al ensayo.
En Q2-2015 comenzó el primer ensayo de infección experimental de los perros naive inmunizados en 2014. En este ensayo se ha evaluado el mantenimiento de la respuesta inducida por la vacuna tras la infección y la protección frente al desarrollo de la enfermedad. Los resultados obtenidos han sido exitosos. El parásito no ha sido capaz de revertir la respuesta inmune deseada, inducida por la vacunación.
Además, la vacuna BNT005 ha sido capaz de detener el desarrollo de la enfermedad en el 100% de los perros vacunados 10 meses tras la infección experimental, mientras que el 67% de los perros control han desarrollado la enfermedad entre los meses 6 y 10 tras la infección experimental.
Estos resultados y nuevas pruebas de hipersensibilidad retardada en perros del ensayo de 2013 muestran que la vacuna induce células específicas de memoria con capacidad de proteger durante un largo periodo de tiempo, superior a un año, avalando la promoción del producto hacia fases más cercanas a la solicitud de registro.
En un resultado notable, todas las propiedades de la vacuna no dependen de que se formule con adyuvante. Los ensayos han sido validados y monitoreados por una compañía multinacional, con la que se planifica conjuntamente un ensayo final de eficacia frente a infección natural con alto número de individuos en zona endémica.
Los datos están siendo actualmente sometidos a un proceso de Due Diligence externo con el objeto de formalizar el marco del acuerdo de codesarrollo, registro y licencia comercial.
Recordemos que el medicamento de VIRBAC o el Jarabe que hay actualmente para la Leishmaniasis no son efectivos.
Esto es lo que actualmente se comenta de la vacuna de VIRBAC canelish, que no funciona y competiría con BIONATURIS.
La vacuna protege frente a la enfermedad clínica, NO FRENTE AL CONTAGIO.
Por tanto UN PERRO VACUNADO PUEDEN ENFERMAR DE LEISHMANIA.
El Protocolo de aplicación es el siguiente: previo análisis para descartar que el perro esté infectado ya por leishmania el calendario de vacunación consiste en una primovacunación ( a partir de los 6 meses de edad ) en la que se pondrán 3 dosis de vacuna separadas a inteRvalos de 3 semanas cada dosis.
La inmunidad final aparece 4 semanas después de la última dosis. Después será necesaria una revacunación anual una sola dosis para mantener la inmunidad.
Precio aproximado:
El precio del test es de 25 €.
El precio de cada dosis de vacuna es de 54 € por dosis.
Test y las tres dosis de la primera vacunación por: 187,00€
Las únicas forma de PREVENIR EL CONTAGIO son PIPETAS Y COLLARES que impiden que el flebótomo pique a tu perro, por tanto ni la vacuna ni el jarabe PREVIENEN EL CONTAGIO.
Este hecho se puede ver en el siguiente articulo: http://uprocanes.es/la-polemica-sobre-la-vacuna-de-la-leishmaniosis/
El avance notificado por la compañía es importante, por lo que la vacuna esta ya a punto de dar el paso al registro previo, el acuerdo de licencia puede ser inminente.
En el 1º año de comercialización en EUROPA Canelish vendió un total de 1 millón de dosis de la vacuna y se vacunaron 300,000 perros (se necesitan 3 dosis por perro) http://argos.portalveterinaria.com/pdf/bionews_10.pdf
Por ello dando un precio medio de unos 40€ se podría cifrar en EUROPA en unos 40 millones de € , a esto habría que añadir EEUU ,Brasil y Asia, por ello podríamos determinar unas ventas globales de mas de 150 millones de €.
Pues bien, el BNT05 competiría con canelish y el jarabe, de ser efectiva como indican podría tener una penetración importante porque tanto el Jarabe como la vacuna de Virbac no valen y los medicamentos como veréis no son baratos…
Teniendo en cuenta una tasa de penetración del producto de un 30-40% de cuota de mercado, se estimaría en 45-60 millones las ventas a nivel global, de los cuales un 12,5% neto anual iría a parar a la caja de BIONATURIS.
Esto supondría fácil para BIONATURIS entre 5 y 7,5 millones de € netos al año para la compañía.
La aprobación según el modelo standart de valoración y nuestras cuentas dicen que el acuerdo de licencia y comercialización supondrían un incremento de valor de BIONATURIS en bolsa de al menos 60 millones de €, es decir unos 11€ por acción.
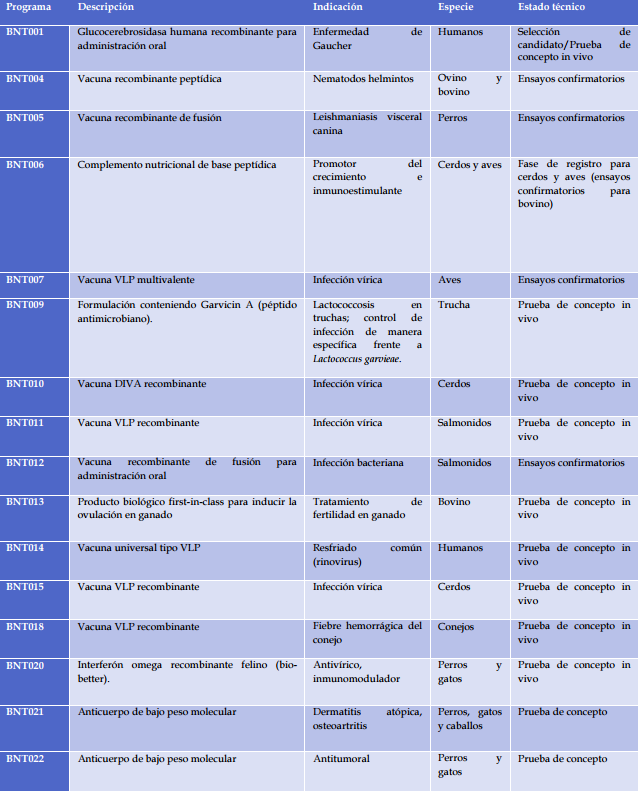
Resto de Portfolio y detalle de “los Top”
De todos ellos destacan los siguientes:
De los productos incluidos en la tabla anterior 11 programas se encuentran en fase de prueba de concepto, 4 en fase de ensayos confirmatorios y 1 en fase de registro y comercialización.
BNT006 (péptido antimicrobiano). Complejo inmunomodulador basado en un péptido que induce la maduración del sistema inmune en animales jóvenes y muestra poder antimicrobiano para combatir infecciones y sus efectos sin el uso de antibióticos o esteroides, incluyendo bacterias multirresistentes. Uso aislado o de manera combinada con otros agentes bactericidas o probióticos. Aplicación en salud humana y animal.
Aunque los resultados en ensayos in vitro mostraron el mismo efecto bactericida que una referencia comercial, los resultados in vivo mostraron una actividad general 7 inmunoestimulante, responsable del incremento de parámetros de crecimiento y disminución de señales de estrés en los animales.
El producto ha sido registrado en México como aditivo alimentario para su uso en granjas de pollos y cerdos y se ha iniciado el proceso de registro en China.
Los resultados en granjas experimentales y comerciales completados muestran que el tratamiento vía oral de animales jóvenes mejora la economía del proceso de producción ya que el conjunto de los animales alcanzan los pesos deseados para su comercialización en menos tiempo y con mejores índices de conversión alimenticia. El efecto se consigue mediante la inducción de la maduración del sistema inmune de los animales más débiles mediante un mecanismo natural bien caracterizado.
En Q4-2015 comenzaron ensayos exploratorios en bovino en colaboración con COVAP (proyecto bovihealth), para confirmar el mantenimiento en rumiantes de estas propiedades observadas tras tratamiento oral de aves y cerdos.
BNT012 es una vacuna contra una importante enfermedad bacteriana en salmónidos y es objeto de un acuerdo de evaluación y opciones con una importante multinacional veterinaria, que está realizando los ensayos de evaluación en granjas experimentales de salmones tras el desarrollo de la fabricación en Bionaturis. Los resultados finalizados en 2014 mostraron seguridad y eficacia en la reducción significativa de la enfermedad en salmones infectados experimentalmente. Sin embargo, se detectó la necesidad de ajustar la dosis para aumentar el efecto de la vacunación en la supervivencia de los salmones retados. En la primera mitad de 2015 Bionaturis optimizó la fabricación de lotes y comenzó el segundo ensayo en salmones en las instalaciones homologadas (Chile) del sponsor. El ensayo finalizó en Q4-2015 como estaba planeado con resultados satisfactorios. Actualmente se están ejecutando pruebas de formulación final para diseñar la estrategia de registro.
BNT013 (tratamiento fertilidad del ganado). Medicamento novedoso fabricado mediante FLYLIFE, dirigido a inducir la ovulación del ganado previo a la inseminación artificial. Objeto de un contrato de desarrollo con una multinacional veterinaria, Bionaturis ejecuta las pruebas de eficacia y seguridad del nuevo fármaco en modelos animales, mientras que la multinacional se encarga de validar estos resultados en sus instalaciones en ensayos de campo con la especie objetivo. El acuerdo incluye opciones de derecho de licencia en exclusiva a favor de la compañía multinacional.
El producto ha sido objeto de una primera fase de desarrollo del proceso de fabricación en Bionaturis, que terminó mostrando que BNT013 es una nueva entidad biológica con las propiedades fisicoquímicas esperadas. En una segunda fase se analizó la actividad biológica del principio activo sin formular. Las pruebas se realizaron sobre tejido derivado de gónadas animales y fueron ejecutados por uno de los principales expertos en reproducción en España. Mostraron que esta nueva molécula de diseño, primera en su género y desarrollada completamente en Bionaturis, posee actividad inductora de la producción de testosterona, progesterona y estradiol, similar o superior que las hormonas naturales. Los ensayos de conformación se han completado con éxito en colaboración con un experto en hormonas de la reproducción en Francia. BNT013 está en fase de análisis de actividad in vivo, en un modelo murino validado por Farmacopea Europea en primer lugar para pasar a un análisis en la especie objetivo, bovino. Los primeros resultados de ovulación en animales modelo, completados en 2015, mostraron la necesidad de formulación galénica para estabilizar la molécula bioactiva.
_Resultados 2015 en línea con las previsiones.
El jueves 7 de abril ofreció un avance de resultados en línea con lo publicado en noviembre. (https://www.gesprobolsa.com/bionaturis-avanza-resultados-sin-novedades/ )
Según el informe del auditor los resultados han estado en línea con el avance de comienzos de abril, es decir sin “sorpresas”
Con esta financiación el Grupo puede hacer frente a las necesidades de inversión en Gastos de I+D para mantener y ampliar su capacidad tecnológica.
Situación de balance.
Patrimonio neto: 5.491.000€
Activo Corriente: 3.300.000€
Pasivo Corriente: 1.674.000€
Fondo de maniobra: +1.626.000€
Deuda financiera a largo plazo: 5.227.000€
Deuda financiera a corto plazo: 841.000€
Efectivo y otros medios líquidos equivalentes: 1.350.000€
Total de deuda financiera neta: +4.718.000€
En deudores comerciales y otras cuentas a cobrar figuran 1.897.000€ por lo siguiente:
El pago pendiente de 1,1 millones de € por uso de Flylife se va a cobrar a plazos mensuales de 40.000€ , de hecho ya se ha cobrado en 2016 varios plazos y el calendario de pagos termina en diciembre de 2017.
Es importante por que así no hay que aprovisionarlo.
Por contra se esta reclamando 850.000€ de la “señal” de la No compra, Bionaturis ha contratado a KPMG y estima recuperable ese importe, por ello no requirió provisionarlo.
Con todo ello la deuda para nada es preocupante y cuenta con liquidez suficiente a corto plazo para hacer frente a los vencimientos de deuda.
Nota: El informe enviado incluye las cuentas individuales y las consolidadas. Las que interesan que son las consolidadas (incluye la filial BIOBIDE) estan a partir de la pagina 46.
https://www.bolsasymercados.es/mab/documentos/InfFinanciera/2016/04/84980_InfFinan_20160430.pdf